臨床試験・治験に特有の仕組み
臨床試験・治験は医学の進歩のためには欠かせないものですが、新しい薬や機器の有効性や安全性は、どのようにして確かめられるのでしょうか。ここでは、科学的に正確な結果を得るために必要とされる試験の仕組みについてご説明します。(なお、「臨床試験・治験とは」のページでも触れているように、治験は臨床試験の一部に含まれているので、両者に共通の内容については「臨床試験」として説明をします。)
臨床試験の3つのステップ
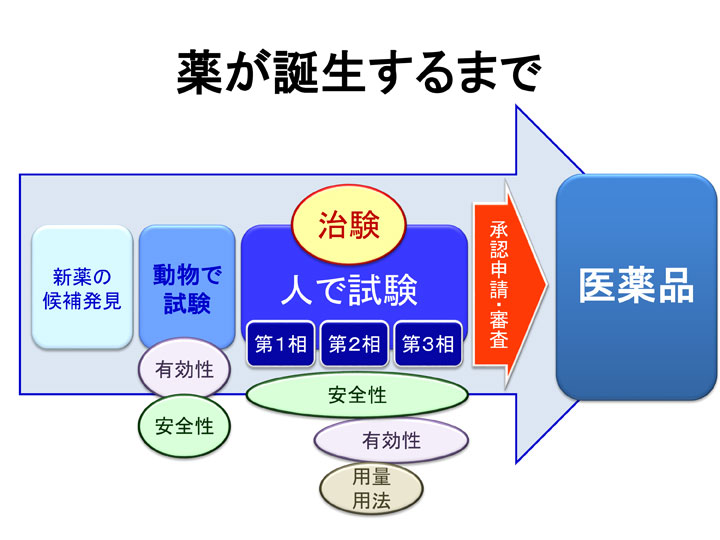 医薬品や医療機器の開発には長い時間がかかります。薬のもとになりそうな化学物質が見つかっても、すぐに人間に使えるわけではなく、まず動物を使って実験します。人を対象とした臨床試験の段階に入っても、厳密な仕組みに従って、少数の患者さんから試験を進めていくことになります。
医薬品や医療機器の開発には長い時間がかかります。薬のもとになりそうな化学物質が見つかっても、すぐに人間に使えるわけではなく、まず動物を使って実験します。人を対象とした臨床試験の段階に入っても、厳密な仕組みに従って、少数の患者さんから試験を進めていくことになります。
この仕組みは複雑ですが、参加者の安全性を確保し、正しい結論を得るために不可欠なものです。特に治験では、新薬の有効性・安全性を正しく評価・検討することが目的なので、第1相、第2相、第3相という3つのステップを踏んで行うことが定められています。
信頼性の高い試験の方法
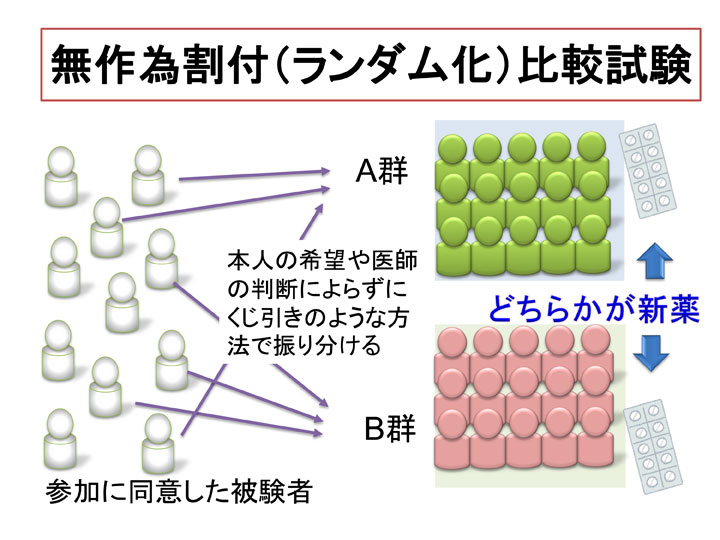 薬や医療機器の有効性・安全性を調べるためには、他の薬(機器)と比べてみる必要があります。それをできる限り科学的に行うための手法として、無作為割付(ランダム化)比較試験と二重盲検試験(目隠し試験)があります。
薬や医療機器の有効性・安全性を調べるためには、他の薬(機器)と比べてみる必要があります。それをできる限り科学的に行うための手法として、無作為割付(ランダム化)比較試験と二重盲検試験(目隠し試験)があります。
無作為割付(ランダム化)とは、患者の意向や医師の判断にはよらないで、乱数表を用いるなどして、くじ引きのような方法で、被験者をグループ分けすることを言います。そうやって、A群・B群それぞれのグループに入る患者さんの体格や体質、健康状態に偏りが生じないようにすることで、新しい薬や医療機器の有効性や安全性を正しく評価できるのです。
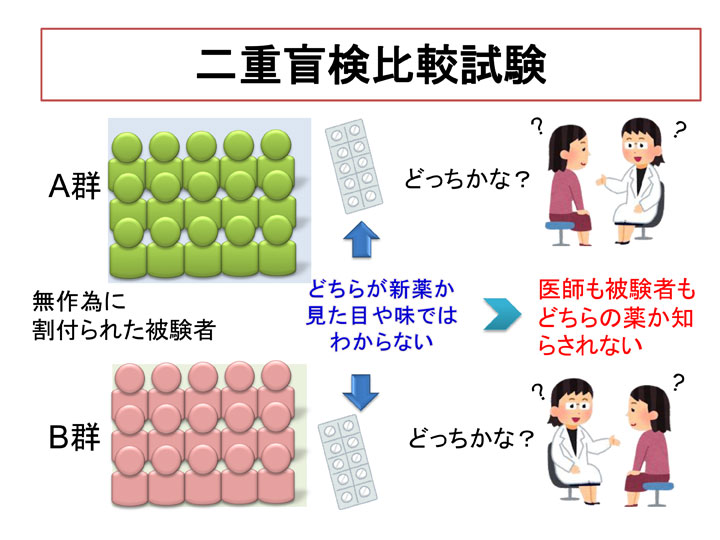 一方、薬の効果は、薬に含まれる化学物質が身体に及ぼす効果(真の薬理効果)に、心理的な期待による効果(プラセボ効果)が加わって現れると言われています。そのような心理的な影響を出来る限り少なくするために、自分が飲んでいる薬が新しい薬かどうかを、本人には知らせないでおくことを「盲検(もうけん)化」といいます。さらに医療者が効果について判定する場合に、患者がどちらのグループに入っているか知っていると、その先入観に影響を受ける(これを観察者バイアスと言います)可能性があるので、医療者にも誰がどのグループに入っているかを知らせない試験(「二重盲検試験」といいます)もあります。
一方、薬の効果は、薬に含まれる化学物質が身体に及ぼす効果(真の薬理効果)に、心理的な期待による効果(プラセボ効果)が加わって現れると言われています。そのような心理的な影響を出来る限り少なくするために、自分が飲んでいる薬が新しい薬かどうかを、本人には知らせないでおくことを「盲検(もうけん)化」といいます。さらに医療者が効果について判定する場合に、患者がどちらのグループに入っているか知っていると、その先入観に影響を受ける(これを観察者バイアスと言います)可能性があるので、医療者にも誰がどのグループに入っているかを知らせない試験(「二重盲検試験」といいます)もあります。
新しい薬を何と比較するのか
新しい薬の効果を知るためには、これまで使用されている薬(既存薬)と比較する方法が一般的です(これを「実薬対照試験」といいます)。しかし、比較をするのに適切な既存薬がない場合に、薬効成分を含まない「プラセボ」と呼ばれるものを使う場合もあります(これを「プラセボ対照試験」といいます)。
プラセボは新しい薬の有効性や安全性を検証する上で、非常に重要な役割を果たしますが、臨床試験でプラセボに当たった人は、試験薬の薬効というメリットは受けられなくなります(逆に副作用というデメリットは回避できることになりますので、一概に「プラセボ=悪」とはいえません)。そのため、世界共通の医学系研究の倫理規範であるヘルシンキ宣言(「臨床試験・治験とは」のページを参照)では、新しい治療法の有効性や安全性を確かめるために比較試験をやるときには、原則的にはその時点で「最善と証明されている治療」と比較するべきとされています。したがって、プラセボを用いる場合は、既存の治療法に試験薬とプラセボをプラスする形が基本となりますが、確立された治療法がない場合や、プラセボが使われても被験者に重大な不利益が及ばないと考えられる場合には単純にプラセボと試験薬だけで比較する試験が行われることがあります。
臨床試験の結果を知る
これまで説明してきたように、新しい薬や治療法が本当にいいのかどうかを検証するのが臨床試験ですが、臨床試験が終わったあとに、自分が当たっていたのはプラセボだったのかどうか、検証されていた新しい薬は国に認可された薬として市場にでたかどうか等、参加した臨床試験の結果を知ることはできるのでしょうか?
2016年11月公開
認定 NPO 法人「健康と病いの語りディペックス・ジャパン」では、一緒に活動をしてくださる方
寄付という形で活動をご支援くださる方を常時大募集しています。

 第1相試験では薬が人体にどういう影響を及ぼすかを調べ、第2相試験で少数の患者を対象に用法・用量を検討し、第3相試験で多くの患者を対象に有効性や安全性を検証する
第1相試験では薬が人体にどういう影響を及ぼすかを調べ、第2相試験で少数の患者を対象に用法・用量を検討し、第3相試験で多くの患者を対象に有効性や安全性を検証する

